Fogli illustrativi digitali in Malesia
Il futuro delle informazioni sui farmaci in Malesia: fogli illustrativi digitali ed etichettatura elettronica
Le informazioni sui prodotti svolgono un ruolo fondamentale nel garantire che i pazienti comprendano i loro trattamenti, supportando al contempo gli operatori sanitari nel loro processo decisionale. Affinché le informazioni sui prodotti diventino più efficaci, nuovi strumenti digitali sono componenti chiave per consentire un uso più efficace dei trattamenti disponibili e contribuire ad aumentare l'alfabetizzazione sanitaria generale. Questi strumenti faciliteranno un accesso più rapido, una migliore comprensione e una migliore fruibilità.
Una tendenza emergente che rientra in questa categoria è l'utilizzo di fogli informativi digitali o etichettatura elettronica. L'etichettatura elettronica è definita come la diffusione di informazioni di prodotto approvate per i medicinali in un formato digitale dinamico che consente lo sviluppo di informazioni di prodotto personalizzate in base alle esigenze dei pazienti e degli operatori sanitari

Circa la metà dei paesi in Asia ha pubblicato informazioni di prodotto in formato PDF sui siti web delle proprie autorità sanitarie (HA). In Malesia, l'etichettatura elettronica è proposta dall'industria dal 2019 per essere in linea con le iniziative di digitalizzazione sanitaria che sono state discusse nell'"International Pharmaceutical Regulators Programme (IPRP)" e nell'"International Conference of Drug Regulatory Authorities (ICDRA)", dove l'etichettatura elettronica è stato uno degli argomenti principali discussi. L'implementazione dell'etichettatura elettronica è in linea con il progresso globale nell'assistenza sanitaria digitale e l'etichettatura elettronica è diventata una delle tendenze emergenti che si sta muovendo a velocità diverse in tutto il mondo. Diversi paesi hanno adottato l'etichettatura elettronica come mezzo per fornire ai pazienti e agli operatori sanitari un facile accesso alle informazioni più recenti sui prodotti.
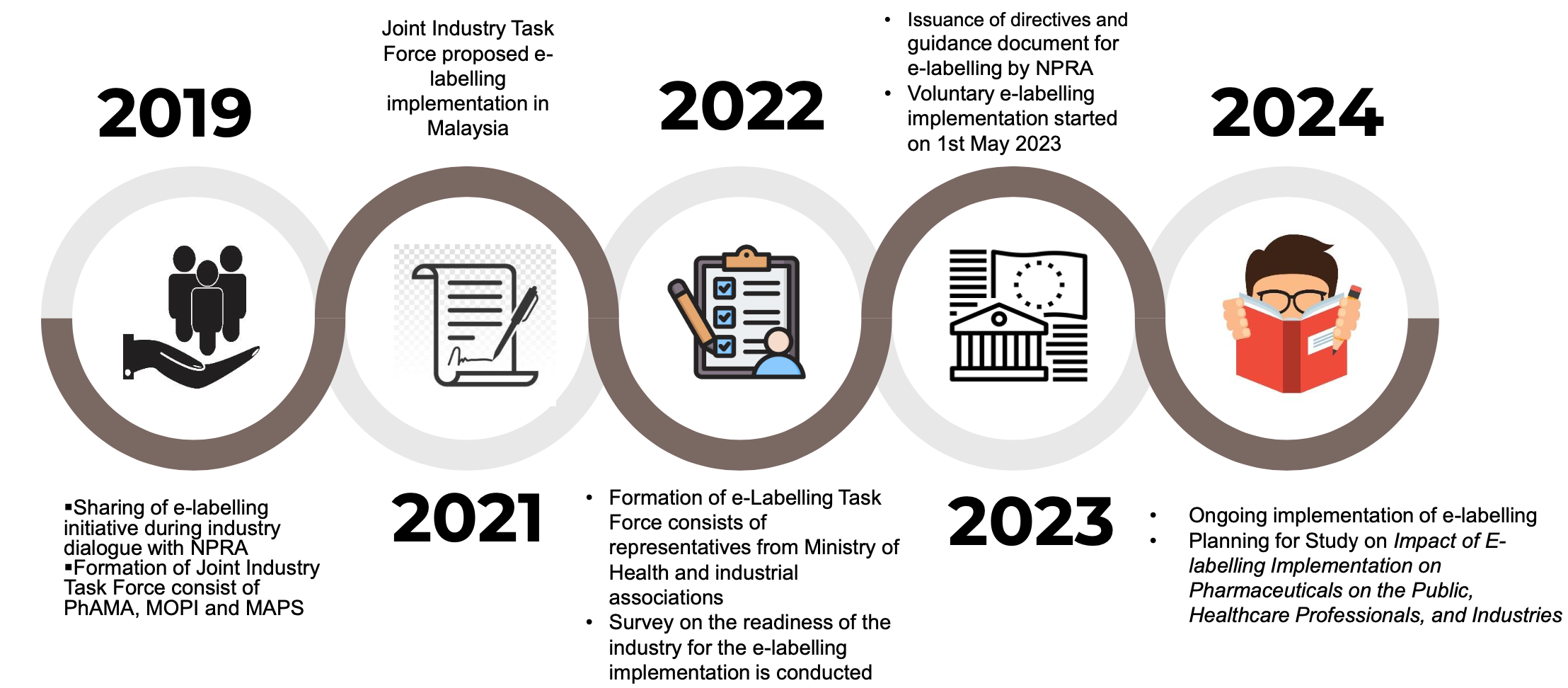
Il percorso dell'etichettatura elettronica in Malesia
Sondaggio sulla capacità del settore: principali risultati
CAPACITA' DI L'IMPLEMENTAZIONE DELL'ETICHETTATURA ELETTRONICA ENTRO IL 3° TRIMESTRE 2022
- 20,5% pronto
- 79,5% non pronto a causa di:
- L'etichetta del prodotto corrente è stata stampata in grandi quantità
- È necessario più tempo per riprogettare l'etichetta per includere il codice QR
- Preoccupazione per il tempo di approvazione delle varianti
- Prontezza del sito di hosting
QUANDO PREVEDETE DI ESSERE PRONTI PER L'IMPLEMENTAZIONE?
- 82,3% pronto per l'implementazione tra il 2023 e il 2025
- 17,7% pronto per l'implementazione entro il terzo trimestre del 2022
QUAL È IL TUO SITO DI HOSTING PER ELEAFLET PREFERITO?
- 52,6% preferito NPRA
- 43,6% preferito azienda o terza parte
- 3,8% non ha preferenze
REQUISITI PER ETICHETTATURA ELETTRONICA IN MALESIA
DEFINIZIONE DI ETICHETTATURA ELETTRONICA
L'etichettatura elettronica è definita come la fornitura di informazioni di prodotto approvate che includono il foglietto illustrativo (PI) e/o il foglietto illustrativo per il consumatore (RiMUP) in formato elettronico tramite un codice Quick Response (QR) leggibile dalla macchina sulla confezione esterna/etichetta interna del prodotto che si collega al sistema NPRA QUEST.
Quando PI e/o RiMUP vengono distribuiti tramite etichettatura elettronica, possono essere distribuite anche copie fisiche stampate con il prodotto. È responsabilità del Titolare della registrazione del prodotto (PRH) fornire le copie fisiche stampate quando richiesto.
TEMPI DI IMPLEMENTAZIONE (VOLONTARIA)
Direttiva di implementazione: 11 aprile 2023 Periodo di implementazione volontaria: 1° maggio 2023 – 31 dicembre 2026
AMBITO DI IMPLEMENTAZIONE
L'implementazione dell'etichettatura elettronica è volontaria e si applica ai nuovi prodotti farmaceutici, biologici e generici contenenti veleni programmati solo per uso umano.
METODO DI IMPLEMENTAZIONE
- Per un nuovo prodotto: come parte del dossier del prodotto.
- Per un prodotto esistente: Notifica di variazione minore
Documento delle linee guida: LINEE GUIDA SULL'ETICHETTATURA ELETTRONICA (ETICHETTATURA ELETTRONICA) PER PRODOTTI FARMACEUTICI IN MALAYSIA
SUPPORTO DATI: CODICE QR
- Il codice QR può essere visualizzato sulla scatola esterna o sull'etichetta interna
- Il codice QR può essere stampato o apposto sulla scatola esterna/etichetta interna utilizzando un'etichetta adesiva
FORMATO DATI: PDF
L'etichettatura elettronica deve essere presentata in un codice QR sulla scatola esterna/etichetta interna del prodotto che si traduce nella pagina NPRA QUEST3+ che visualizza le stesse informazioni sul prodotto in formato PDF.
Il formato consentirebbe una visualizzazione ottimizzata su qualsiasi dispositivo elettronico come smartphone/laptop/tablet.
Le informazioni sui prodotti in formato video non sono attualmente consentite
SITO DI HOSTING: SISTEMA NPRA QUEST
La capacità massima delle informazioni sui prodotti (etichettatura elettronica) da caricare e ospitare nel sistema QUEST3+ non deve superare i 5 MB
PASSAGGI SUCCESSIVI
Compatibilità multipiattaforma
La progettazione di soluzioni di etichettatura elettronica compatibili con un'ampia gamma di dispositivi, sistemi operativi e applicazioni software migliora l'interoperabilità.
Formati standardizzati
L'adozione di formati standardizzati per i dati di etichettatura elettronica è essenziale per l'interoperabilità. Formati comuni assicurano che le informazioni possano essere facilmente scambiate e comprese da diversi sistemi e dispositivi
Gestione dei farmaci
- L'integrazione dell'etichettatura elettronica può consentire a operatori sanitari, consumatori e pazienti di accedere elettronicamente a informazioni complete sui farmaci
- Ciò include dettagli quali istruzioni sul dosaggio, controindicazioni e potenziali interazioni farmacologiche
Fonti
- LINEE GUIDA SULL'ETICHETTATURA ELETTRONICA (ETICHETTATURA ELETTRONICA) PER PRODOTTI FARMACEUTICI IN MALESIA
- PhAMA: Associazione farmaceutica della Malesia
- MOPI: Organizzazione malese delle industrie farmaceutiche
- MAPS: Associazione malese dei fornitori farmaceutici