Folletos digitales en Malasia
El futuro de la información sobre medicamentos en Malasia: folletos electrónicos y etiquetado electrónico
Folletos digitales en Malasia El futuro de la información sobre medicamentos en Malasia: folletos electrónicos y etiquetado electrónico
La información sobre los productos desempeña un papel fundamental para garantizar que los pacientes comprendan sus tratamientos y, al mismo tiempo, para ayudar a los profesionales sanitarios a tomar decisiones. Para que la información sobre los productos sea más eficaz, las nuevas herramientas digitales son componentes clave que permiten un uso más eficaz de los tratamientos disponibles y ayudan a aumentar la alfabetización sanitaria general. Estas herramientas facilitarán un acceso más rápido, una mejor comprensión y una mayor facilidad de uso.
Una tendencia emergente que encaja en esta categoría es el etiquetado electrónico. El etiquetado electrónico se define como la difusión de información aprobada sobre productos medicinales en un formato digital dinámico que permite el desarrollo de información personalizada sobre productos en función de las necesidades de los pacientes y los profesionales sanitarios.

Aproximadamente la mitad de los países de Asia han publicado información sobre productos en formato PDF en los sitios web de sus Autoridades Sanitarias (HA). En Malasia, la industria propone el etiquetado electrónico desde 2019 para estar en línea con las iniciativas de digitalización de la atención sanitaria que se discutieron en el Programa Internacional de Reguladores Farmacéuticos (IPRP) y la Conferencia Internacional de Autoridades Reguladoras de Medicamentos (ICDRA), donde el etiquetado electrónico y la confianza han sido los principales temas debatidos. La implementación del etiquetado electrónico está en línea con el avance global en la atención sanitaria digital y el etiquetado electrónico se ha convertido en una de las tendencias emergentes que se mueve a diferentes velocidades en todo el mundo. Varios países han adoptado el etiquetado electrónico como medio para proporcionar a los pacientes y profesionales sanitarios un acceso fácil a la información más reciente sobre los productos.
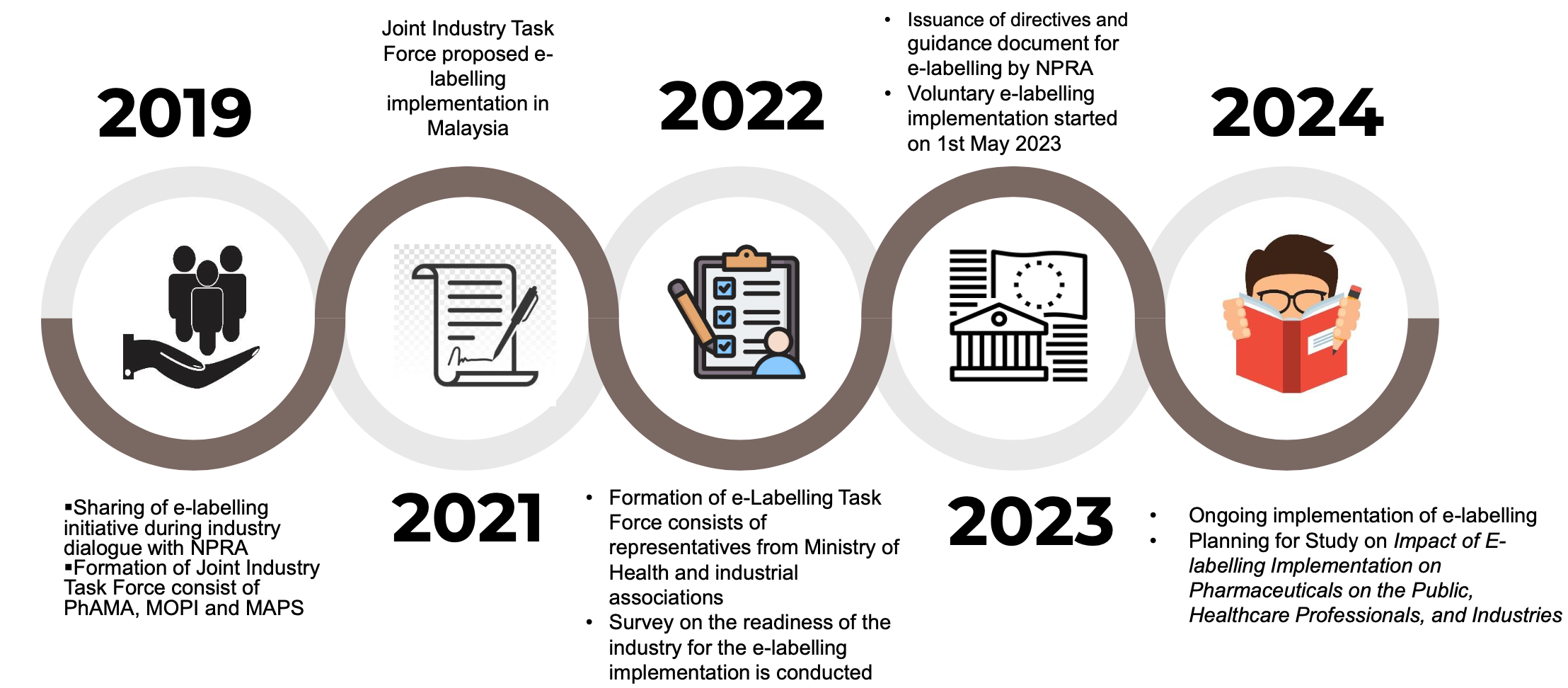
Hitos del etiquetado electrónico en Malasia
Encuesta sobre la preparación de la industria: principales hallazgos
PREPARACIÓN PARA LA IMPLEMENTACIÓN DEL ETIQUETADO ELECTRÓNICO PARA EL TERCER TRIMESTRE DE 2022
- 20,5 % listo
- 79,5 % no listo debido a:
- La etiqueta actual del producto se ha impreso en gran cantidad
- Se necesita más tiempo para rediseñar la etiqueta para incluir el código QR
- Preocupación por el tiempo de aprobación de la variación
- La preparación del sitio de alojamiento
¿CUÁNDO PREVÉ QUE SE PODRÍA ALCANZAR LA PREPARACIÓN?
- 82,3 % listo para implementar entre 2023 y 2025
- 17,7 % listo para implementar en el tercer trimestre de 2022
¿CUÁL ES SU SITIO DE ALOJAMIENTO DE ETIQUETADO ELECTRÓNICO PREFERIDO ?
- 52,6 % prefiere NPRA
- 43,6 % prefiere una empresa o un tercero
- 3,8 % no tiene preferencia
REQUISITOS DE ETIQUETADO ELECTRÓNICO EN MALASIA
DEFINICIÓN DE ETIQUETADO ELECTRÓNICO
El etiquetado electrónico se define como la provisión de información de producto aprobada que incluye el prospecto (PI) y/o el prospecto de información de medicamentos para el consumidor (RiMUP) electrónicamente a través de un código de respuesta rápida (QR) legible por máquina en la caja exterior/etiqueta interior del producto que se vincula al sistema NPRA QUEST.
Cuando el PI y/o el RiMUP se distribuyen mediante etiquetado electrónico, también se pueden distribuir copias impresas físicas junto con el producto. Es responsabilidad del Titular del Registro del Producto (PRH) proporcionar las copias impresas físicas cuando sea necesario.
PLAZO DE IMPLEMENTACIÓN VOLUNTARIA
Directiva de implementación: 11 de abril de 2023 Período de implementación voluntaria: 1 de mayo de 2023 – 31 de diciembre de 2026
ÁMBITO DE IMPLEMENTACIÓN
La implementación del etiquetado electrónico es voluntaria y se aplica a nuevos medicamentos, productos biológicos y genéricos que contengan venenos programados para uso humano únicamente.
MÉTODO DE IMPLEMENTACIÓN
- Para un producto nuevo: como parte del expediente del producto.
- Para un producto existente: Notificación de variación menor
Documento de directrices: GUIDELINE ON ELECTRONIC LABELLING (E-BELLING) FOR PHARMACEUICAL PRODUCTS IN MALAYSIA
SOPORTE DE DATOS: CÓDIGO QR
- El código QR puede mostrarse en la caja exterior o en la etiqueta interior
- El código QR puede imprimirse o colocarse en la caja exterior o en la etiqueta interior mediante una etiqueta adhesiva
FORMATO DE DATOS: PDF
El etiquetado electrónico se presentará en un código QR en la caja exterior o en la etiqueta interior del producto que se traduce a la página NPRA QUEST3+ que muestra la misma información del producto en formato pdf.
El formato permitiría una visualización optimizada en cualquier dispositivo electrónico, como teléfonos inteligentes, computadoras portátiles o tabletas.
Actualmente no se permite la información de productos en formato de video
SITIO DE ALOJAMIENTO: SISTEMA NPRA QUEST
La capacidad máxima de información de productos (etiquetado electrónico) que se cargará y alojará en el sistema QUEST3+ no superará los 5 MB
PRÓXIMOS PASOS
Compatibilidad entre plataformas
El diseño de soluciones de etiquetado electrónico que sean compatibles con una amplia gama de dispositivos, sistemas operativos y aplicaciones de software mejora la interoperabilidad.
Formatos estandarizados
La adopción de formatos estandarizados para los datos de etiquetado electrónico es esencial para la interoperabilidad. Los formatos garantizan que la información pueda intercambiarse y entenderse fácilmente por diferentes sistemas y dispositivos
Gestión de medicamentos
- La integración del etiquetado electrónico puede permitir que los proveedores de atención médica, los consumidores y los pacientes accedan a información completa sobre medicamentos de forma electrónica
- Esto incluye detalles como instrucciones de dosificación, contraindicaciones y posibles interacciones farmacológicas
Fuentes
- DIRECTRICIDAD SOBRE ETIQUETADO ELECTRÓNICO (E-ETIQUETADO) PARA PRODUCTOS FARMACÉUTICOS EN MALASIA
- PhAMA: Asociación farmacéutica de Malasia
- MOPI: Organización de industrias farmacéuticas de Malasia
- MAPS: Asociación de proveedores farmacéuticos de Malasia