La soluzione eLeaflet di myHealthbox ora supporta il formato dati SPL, consentendo così la piena compatibilità con il formato di informazioni digitali FDA per le informazioni sui medicinali e sui prodotti sanitari.

Cos'è l'SPL
Lo Structured Product Labelling (SPL) è uno standard di markup dei documenti approvato da Health Level Seven (HL7) e adottato dalla FDA come meccanismo per lo scambio di informazioni su prodotti e strutture.

Structured Product Labelling (SPL) è uno standard Health Level Seven (HL7) basato su Clinical Document Architecture e HL7 Reference Information Model (RIM) accreditato dall'American National Standards Institute (ANSI) per lo scambio di informazioni sui prodotti. I documenti di etichettatura dei prodotti strutturati includono un'intestazione e un corpo. L'intestazione include informazioni sul documento come il tipo di prodotto, l'autore e il controllo delle versioni. Il corpo del documento include informazioni sul prodotto sia in formato testo strutturato che in formato elemento dati. La Food and Drug Administration (FDA) degli Stati Uniti utilizza i documenti SPL per scambiare informazioni su un numero crescente di argomenti relativi ai prodotti.
Cosa significa ?
Molto semplicemente è ora possibile importare prodotti registrati FDA in formato SPL direttamente nella nostra piattaforma eLeaflet rendendo così la creazione di un eLeaflet da un prodotto con un file di dati SPL facile e completamente automatica.
Qual è la differenza tra eLeaflet e SPL
Prima di tutto è importante chiarire che pur condividendo molte somiglianze sia dal punto di vista della struttura dei dati che del design, i due formati risolvono 2 problemi molto diversi e sono originati da una prospettiva diversa nel problema più ampio del miglioramento delle informazioni sui prodotti in ambito sanitario tramite soluzioni digitali.
Entrambe sono rappresentazioni strutturate di dati e in particolare di dati di informazioni sul prodotto ed entrambe sono destinate a prodotti sanitari. Entrambi sono basati su XML.
È possibile ottenere l'interoperabilità tra i due formati, come dimostra il nostro recente supporto per SPL nell'eLeaflet.
Le differenze
Il focus di SPL e la principale motivazione per la sua adozione è il miglioramento del ciclo di gestione normativa (data editing, revisione, approvazione). L'idea alla base era quella di sostituire il formato MS Word che era (ed è ancora) ampiamente utilizzato durante il processo di autorizzazione all'immissione in commercio per lo scambio di informazioni tra la FDA e il titolare dell'autorizzazione all'immissione in commercio o il produttore.
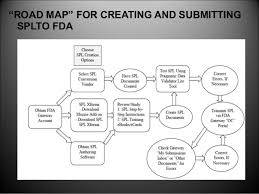
Dall'altra parte invece l'obiettivo e la motivazione principale alla base dello sviluppo dell'eLeaflet è la sostituzione e il miglioramento del foglio informativo cartaceo che viene solitamente inserito nelle confezioni dei medicinali. L'idea è di migliorare l'esperienza per l'utente finale (pazienti od operatori sanitari), migliorare l'accessibilità e la scoperta dei contenuti e aprire la strada a funzionalità innovative.
Mentre tutte le funzionalità di definizione dei contenuti che sono presenti nell'SPL si trovano anche nell'eLeaflet, quest'ultimo consente la definizione di elementi dinamici e interattivi che mancano nella definizione dell'SPL.
L'eLeaflet è progettato anche per un'ampia distribuzione e funzionalità come la sicurezza dei contenuti, le firme digitali, l'autenticazione notarile, la garanzia dei contenuti e l'incapsulamento sono caratteristiche standard come richiesto tipicamente da soluzioni per il mondo farmaceutico che sono fortemente regolamentate ed accessibili da milioni di persone.
Esempi
Alcuni esempi di eLeaflet generato da un SPL sono disponibili qui:
Ulteriori informazioni sulla soluzione eLeaflet di myHealthbox sono disponibili sul sito eLeaflet